
清空記錄
歷史記錄
取消
清空記錄
歷史記錄



氨基酸賦能生物藥【二】:組氨酸如何守護抗體藥物穩定性
目前已有超過 40% 獲得市場批準的單克隆抗體在其配方中添加了組氨酸和鹽酸組氨酸,在基于蛋白質的生物制劑配方中,常用的組氨酸濃度范圍為10 mM~20 mM,已知的最低使用濃度為3 mM(bamlanivimab,pH 6.0),最高使用濃度可達50 mM(Takhzyro?,pH 6.0,Entyvio?,pH 6.3)[1]。
組氨酸的結構可分為三個主要部分(見圖1):α-羧基(pKa 1.8)、α-氨基(pKa 9.2)和咪唑側鏈(pKa 6.0)。咪唑基團是一種很強的親核基團,能夠快速提供與接受質子,在中性環境中,組氨酸不帶電,表現出疏水特性,而當pH< pKa 時,組氨酸質子化帶正電,轉變為親水性分子。
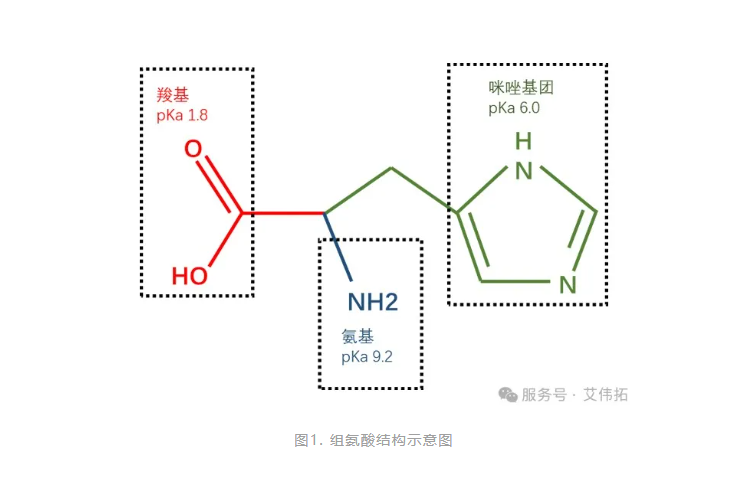
在基于蛋白質的生物制劑中,組氨酸通常起到pH調節劑、蛋白質穩定劑、抗氧化劑、降粘劑及增溶劑的作用:
01pH調節劑
溶液pH會通過改變氨基酸側鏈的電荷狀態、破壞或形成非共價相互作用、甚至引發共價修飾等方式對氨基酸殘基的化學完整性以及蛋白質高級結構的折疊等多種性質產生深遠影響,緩沖液可用于控制溶液的 pH值。為了獲得更好的緩沖效果,緩沖液的pH值應控制在緩沖劑 pKa 值的1個pH單位范圍內。組氨酸的 pKa 約為 6.0,能夠使組氨酸緩沖液的pH值保持在5.5至6.5之間。然而,由于配方中存在其他輔料,組氨酸實際的緩沖范圍更更寬(pH 5.0 ~6.9)。在實際生產過程中,組氨酸常與鹽酸組氨酸共同發揮作用,如表1所示,部分獲批抗體制劑配方中,組氨酸與鹽酸組氨酸總是成對出現。

02蛋白穩定劑
組氨酸還可以直接作為多種基于蛋白質的生物制劑配方的良好穩定劑。蛋白質的物理穩定性包括構象穩定性、膠體穩定性和界面穩定性。輔料的添加通常會對蛋白質的穩定性產生不止一種影響。與其他緩沖劑相比,組氨酸有助于提高構象穩定性和膠體穩定性,維系構象穩定性的主要機制為配體結合。如圖2所示,在濃度、pH值和離子強度完全相同的情況下,組氨酸對干擾素τ制劑的構象穩定作用優于其他緩沖液(如磷酸鹽和Tris)[2]。
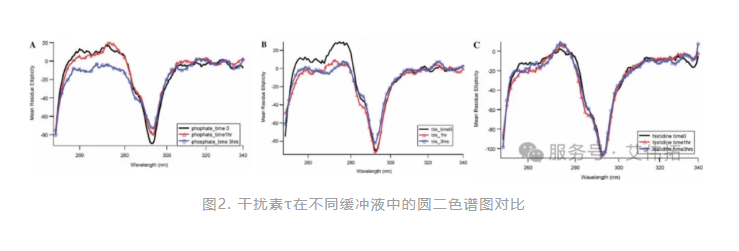
膠體穩定性涉及蛋白質-蛋白質相互作用,其中蛋白質作為典型的膠體,分子間產生凈吸引力或排斥力,因此,膠體穩定性影響蛋白質聚集的傾向。研究表明,組氨酸穩定性的機制與緩沖液分子遮蔽蛋白質表面暴露于溶劑中的疏水區域有關。
此外,組氨酸能通過與其他殘基形成氫鍵,阻止抗體鉸鏈區的裂解,在相同的pH 值和離子強度條件下,與磷酸鹽相比,使用組氨酸作為緩沖劑時,鉸鏈區的水解速率更低。
在某些情況下,液體制劑不夠穩定,將蛋白質制成固態制劑是延長不穩定治療性蛋白質保質期的一種替代方法。然而,在固態制劑的生產過程中,冷凍和干燥階段產生的壓力極易導致蛋白質受損,組氨酸在此過程中則可對蛋白質起到保護作用。因此,組氨酸是蛋白制劑凍干過程中使用最廣泛的氨基酸,其通過形成玻璃狀基質,將蛋白質分子分隔開,并限制蛋白質遷移,從而抑制蛋白質聚集和變性。
03 抗氧化劑
組氨酸還是一種抗氧化劑,能夠清除溶液中的羥基自由基和單線態氧。微量金屬離子,如銅和鐵,通常以雜質的形式存在于藥物制劑中,并能促進蛋白質的氧化。在蛋白質產品的加工和儲存過程中,容器(例如不銹鋼制造設備)也可能滲出具有氧化活性的金屬。由于組氨酸能與這些離子形成強復合物,因此可作為抗氧化劑使用。將組氨酸用作輔料而也能為提高體內抗氧化保護提供一種安全有效的方法。
04 降粘劑
鑒于皮下注射的注射量有限(小于2 mL)以及劑量要求較高(幾百毫克或更多),單克隆抗體有時會以較高濃度配制[3]。FDA批準的單克隆抗體制劑中,有三分之一是高蛋白濃度配制的(100 mg/mL或更高)。在這些獲批的單克隆抗體中,最高蛋白濃度為200 mg/mL。由于膠體蛋白溶液中的蛋白質相互作用,單克隆抗體在高濃度制劑中表現出復雜的溶液特性,如高粘度、高聚集傾向和低穩定性。這些特性嚴重阻礙了用于皮下注射的高濃度單克隆抗體溶液的開發。此外,生物制藥的高粘度使得制劑的最終超濾或透析步驟變的困難。
組氨酸已被證明可通過陽離子-π或π-π堆積相互作用與芳香族殘基相互作用,并有助于降低粘度。當組氨酸作為不同濃度和不同pH值下的輔料使用時,mAb之間的分子間相互作用的大小和水動力學半徑會受到影響。隨著組氨酸濃度的增加,制劑的水動力學半徑增大,在組氨酸濃度約為20 mM時達到峰值。組氨酸對水動力學半徑的影響與溶液粘度和滲透壓的變化有關。這些變化可能是氫鍵、芳香族(例如π堆積)和靜電相互作用的結果。例如,在150 mg/mL的全人源ABX-IL8中,40 mM組氨酸可使粘度減半。因此,在弱酸性條件下,添加組氨酸是降低高濃度蛋白質溶液粘度的良好選擇,組氨酸鹽酸鹽則是降低高濃度蛋白制劑粘度的首選鹽。
05 增溶劑
溶解度不足是藥物開發過程中常見的瓶頸,研究表明組氨酸可提高大豆蛋白的溶解度。大豆蛋白是一種常用的活性成分。無論鹽濃度如何,加入組氨酸都能提高大豆蛋白的溶解度并降低其濁度(圖3)[4]。
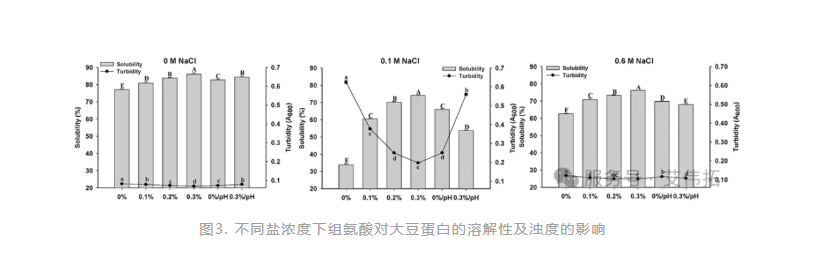
除卻以上作為生物制劑配方中的組分之外,組氨酸還可用于色譜法純化和分析單克隆抗體的洗脫液,在洗脫緩沖液中添加組氨酸可以提高單克隆抗體(mAbs)色譜純化的雜質清除率。
參考文獻:
[1] Robert G. Strickleya,, William J. Lambertb, A review of formulations of commercially available antibodies. Journal of Pharmaceutical Sciences.2021,2590-2608
[2] Katayama, et al. Effect of Buffer Species on the Thermally Induced Aggregation of Interferon-tau, Journal of Pharmaceutical Sciences, 2006,95,6
[3] Shawn Shouye Wang,, Yifei (Susie) Yan and Kin Ho, US FDA-approved therapeutic antibodies with high-concentration formulation: summaries and perspectives,Antibody Therapeutics, 2021, 4, 262–273
[4] Wang, Y., Ma, T., Liu, C., Guo, F., Zhao, J. L-Histidine improves solubility and emulsifying properties of soy proteins under various ionic strengths. LWT ,2021,152, 112382.
艾偉拓4款注射級氨基酸輔料已全部完成主流藥典(USP,EP,ChP等)符合性研究,更在關鍵指標上實現超越,全面對標一線進口品牌,已廣泛供應眾多生物醫藥企業,為生物制劑的穩定性和安全性保駕護航,為國產創新藥的中外申報提供助力!

艾偉拓致力于為客戶提供更優質的服務,不僅提供藥典符合性聲明,還能單獨出具符合具體藥典標準的檢測報告(COA)。如果您有任何需求或疑問,歡迎掃描下方二維碼添加客服,或聯系您所在區域的銷售人員,我們將竭誠為您解答和服務。
生物制品穩定劑,國產保供認準AVT!



 瀏覽器自帶分享功能也很好用哦~
瀏覽器自帶分享功能也很好用哦~




